Anaplasmose (hond): verschil tussen versies
(→Specifiek) |
(→Specifiek) |
||
| Regel 79: | Regel 79: | ||
**seroconversie meest betrouwbaar 3w na infectie maar symptomen kunnen eerder optreden en kan maanden tot jaren persisteren na herstel. | **seroconversie meest betrouwbaar 3w na infectie maar symptomen kunnen eerder optreden en kan maanden tot jaren persisteren na herstel. | ||
**Negatieve resultaten sluiten een actieve anaplasmose niet uit bij acuut zieke dieren. | **Negatieve resultaten sluiten een actieve anaplasmose niet uit bij acuut zieke dieren. | ||
| − | **Positieve resultaten correleren niet noodzakelijk met ziekte bij klinische gezonde dieren. Desalniettemin wordt aanbevolen de [[thrombocytentelling]] op te volgen. | + | **Positieve resultaten correleren niet noodzakelijk met ziekte bij klinische gezonde dieren. Desalniettemin wordt aanbevolen de [[thrombocyten|thrombocytentelling]] op te volgen. |
*'''PCR''' | *'''PCR''' | ||
Versie van 29 mei 2015 om 16:24
Anaplasmose bij honden wordt veroorzaakt door A. phagocytophilum en A. platys, Gram negatieve, obligaat intracellulaire bacteriën die samen met Ehrlichia en Neorickettsia tot de familie van de Anaplasmataceae behoren.[1]. Beide species verschillen in vector, tropisme en ziektebeeld.
| Species | Vector | Tropisme | Ziektebeeld | Synoniemen |
|---|---|---|---|---|
| A. phagocytophilum | Ixodes | Granulocyten | Canine granulocytotropische anaplasmose | Ehrlichia equi, Ehrlichia phagocytophila, human granulocytic ehrlichiosis (HGE) agent |
| A. platys | Rhipicephalus | Thrombocyten | Cyclische thrombocytopenie |
A. phagocytophilum
Levenscyclus
- Grote verscheidenheid gastheren maar georganiseerd in ecotypes. Stammen die honden infecteren, infecteren ook mensen, runderen en paarden.[2] (Schema)
- Reservoir: wildlife (herten, egels, knaagdieren, vogels...)
- De bacterie handhaaft zich in granulocyten.
Zowel larven, nymfen als volwassen Ixodes teken (her)infecteren zich tijdens een bloedmaaltijd en brengen de rickettsen ook weer over naar hun gastheer. Er is geen transoveriële overdracht. A. phagocytophilum wordt beschouwd als één species maar tijdens kruisinfectie experimenten bleken isolaten afkomstig van een bepaald type gastheer niet infectieus voor een heterologe gastheer. Nader onderzoek bracht 4 ecotypes aan het licht waarbij ecotype I circuleert bij mens en gedomesticeerde dieren.[2]
De ziekte
Verspreiding
- Tekenbeet. De overdracht gebeurt evenwel niet onmiddellijk, maar geschiedt pas ongeveer 24 tot 48 uur nadat de teek zich heeft vastgehecht.
- Besmetting via bloed-bloed contact is mogelijk, bloed subinoculatie wordt bovendien aangewend in experimenten.
- Iatrogene transmissie dmv transfusie en chirurgisch materiaal is gemeld bij de mens.
- Perinatale en transplacentale transmissie werden beschreven bij resp mens en rund maar niet bij honden.[3]
Epidemiologie
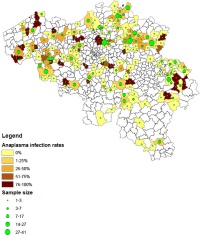
Ongeveer 20% van de Ixodes teken in België zijn positief voor A. phagocytophilum![4] Er zijn klinische gevallen beschreven bij mens en runderen en tevens geïmporteerde honden, maar gezien de hoge tekenbesmettingsgraad blijven velen vermoedelijk ongediagnosticeerd.
Door het vele reizen ziet men ook een toename van het voorkomen in niet-endemische gebieden. Het besmettingsrisico volgt die van de tekenpopulaties waardoor verspreiding door heel Europa mogelijk is!
Ziekteverloop
Symptomen
- lethargie
- koorts
- anorexie
- neutrofiele polyarthritis
- diarree, braken
- opgezette lnn.
- petechiën, epistaxis
Pathologische veranderingen
- splenomegalie
- lymfoïde hyperplasie
In endemische gebieden waar vele honden seropositief zijn, vertonen de meesten geen enkel symptoom.[5][6]
Infectie wordt geacht zelflimiterend te zijn maar heropflakkering na immunosupressieve therapie werd beschreven.[7][8]
Diagnose
Aspecifiek
- afwijkingen CBC
- thrombocytopenie (meestal)
- milde anemie, regeneratief of niet
- lymfopenie
- hypoalbuminemia
- hyperglobulinemia
- ALP verhoogd
Specifiek
- in een bloeduitstrijkje kunnen morulae zichtbaar zijn in granulocyten van acute gevallen. Deze zijn microscopisch niet te onderscheiden van Ehrlichia.
- seroconversie meest betrouwbaar 3w na infectie maar symptomen kunnen eerder optreden en kan maanden tot jaren persisteren na herstel.
- Negatieve resultaten sluiten een actieve anaplasmose niet uit bij acuut zieke dieren.
- Positieve resultaten correleren niet noodzakelijk met ziekte bij klinische gezonde dieren. Desalniettemin wordt aanbevolen de thrombocytentelling op te volgen.
- PCR
A. platys
Levenscyclus
De cyclus van A. platys is nog grotendeels onbekend. Honden en recentelijk ook vossen[9] kunnen besmet worden vermoedelijk via R. sanguineus[10], een tekensoort met een sterke voorkeur voor honden.
- De hond zelf wordt als belangrijkste reservoir aanzien.
- De bacterie handhaaft zich in thrombocyten.
De ziekte
Verspreiding
idem A. phagocytophilum
Epidemiologie
A. platys werd in Belgie zelf nog niet aangetroffen, wel in Spanje[11], Kroatië[12] en tropische gebieden met sterke Rhipicephalus sanguineus infestatiedruk.
Ziekteverloop
Symptomen
- meestal zonder, ondanks erge thrombocytopenie.
- bloedingsneiging[13]
- uveitis anterior (1 rapport [14])
Symptomen kunnen wel makkelijker optreden bij co-infectie met andere vector-overdraagbare pathogenen zoals E. canis[15][16]
Diagnose
Aspecifiek
- afwijkingen CBC
- thrombocytopenie
- niet-regeneratieve anemie
- leukopenie
- hypoalbuminemie
- hypergammaglobulinemie
- hypocalcemie
Specifiek
- in een bloeduitstrijkje kunnen morulae zichtbaar zijn in bloedplaatjes maar zijn soms moeilijk te onderscheiden van thrombocytengranules.
- Serologie
- seroconversie meest betrouwbaar 3w na infectie maar symptomen kunnen eerder optreden en kan maanden tot jaren persisteren na herstel.
- Negatieve resultaten sluiten een actieve anaplasmose niet uit bij acuut zieke dieren.
- Positieve resultaten correleren niet noodzakelijk met ziekte bij klinische gezonde dieren. Desalniettemin wordt aanbevolen de thrombocytentelling op te volgen.
- PCR
Referenties
- ↑ Dumler et al.: Reorganization of genera in the families Rickettsiaceae and Anaplasmataceae in the order Rickettsiales: unification of some species of Ehrlichia with Anaplasma, Cowdria with Ehrlichia and Ehrlichia with Neorickettsia, descriptions of six new species combinations and designation of Ehrlichia equi and 'HGE agent' as subjective synonyms of Ehrlichia phagocytophila. Int. J. Syst. Evol. Microbiol. 2001;51:2145-65. PMID: 11760958.
- ↑ 2,0 2,1 Jahfari et al.: Circulation of four Anaplasma phagocytophilum ecotypes in Europe. Parasit Vectors 2014;7:365. PMID: 25127547. DOI.
- ↑ Plier et al.: Lack of evidence for perinatal transmission of canine granulocytic anaplasmosis from a bitch to her offspring. J Am Anim Hosp Assoc 2009;45:232-8. PMID: 19723846. DOI.
- ↑ Claerebout et al.: Ticks and associated pathogens collected from dogs and cats in Belgium. Parasit Vectors 2013;6:183. PMID: 23777784. DOI.
- ↑ Beall et al.: Serological and molecular prevalence of Borrelia burgdorferi, Anaplasma phagocytophilum, and Ehrlichia species in dogs from Minnesota. Vector Borne Zoonotic Dis. 2008;8:455-64. PMID: 18302532. DOI.
- ↑ Bowman et al.: Prevalence and geographic distribution of Dirofilaria immitis, Borrelia burgdorferi, Ehrlichia canis, and Anaplasma phagocytophilum in dogs in the United States: results of a national clinic-based serologic survey. Vet. Parasitol. 2009;160:138-48. PMID: 19150176. DOI.
- ↑ Egenvall et al.: Detection of granulocytic Ehrlichia species DNA by PCR in persistently infected dogs. Vet. Rec. 2000;146:186-90. PMID: 10718591.
- ↑ Alleman AR, Chandrashekar R, Beall M. Experimental inoculation of dogs with a human isolate (NY18) of Anaplasma phagocytophilum and demonstration of persistent infection following doxycycline therapy [abstract]. J Vet Intern Med 2006;20:763.
- ↑ Cardoso et al.: First report of Anaplasma platys infection in red foxes (Vulpes vulpes) and molecular detection of Ehrlichia canis and Leishmania infantum in foxes from Portugal. Parasit Vectors 2015;8:144. PMID: 25889750. DOI.
- ↑ Ramos et al.: Detection of Anaplasma platys in dogs and Rhipicephalus sanguineus group ticks by a quantitative real-time PCR. Vet. Parasitol. 2014;205:285-8. PMID: 25027609. DOI.
- ↑ Heyman et al.: Molecular and serological evidence for Anaplasma platys and Babesia sp. infection in a dog, imported in Belgium, from Southern Spain. J Vet Med A Physiol Pathol Clin Med 2007;54:276-9. PMID: 17523964. DOI.
- ↑ Dyachenko et al.: First case of Anaplasma platys infection in a dog from Croatia. Parasit Vectors 2012;5:49. PMID: 22401583. DOI.
- ↑ Abarca et al.: Anaplasma platys in dogs, Chile. Emerging Infect. Dis. 2007;13:1392-5. PMID: 18252119. DOI.
- ↑ Glaze & Gaunt: Uveitis associated with Ehrlichia platys infection in a dog. J. Am. Vet. Med. Assoc. 1986;189:916-7. PMID: 3771363.
- ↑ Hua et al.: Canine ehrlichiosis caused simultaneously by Ehrlichia canis and Ehrlichia platys. Microbiol. Immunol. 2000;44:737-9. PMID: 11092236.
- ↑ Gaunt et al.: Experimental infection and co-infection of dogs with Anaplasma platys and Ehrlichia canis: hematologic, serologic and molecular findings. Parasit Vectors 2010;3:33. PMID: 20377870. DOI.
Links
- Anaplasma phagocytophilum PCR
- Vector_overdraagbare_serologie
- Wikipedia
- Microbewiki
- Artikels op Pubmed over honden in de laatste 12 maanden